Parasiten sind Lebewesen, die auf Kosten anderer leben. Sie zapfen den Stoffwechsel ihrer Wirte an und entziehen ihnen Nährstoffe und Energie. Und als sei das nicht genug, schaden sie den Wirtsorganismen zusätzlich, indem sie Giftstoffe produzieren oder zelluläre Schäden verursachen und den Wirt aus der Balance bringen. Das Forschungsteam um Prof. Dr. Ute Hellmich vom Exzellenzcluster »Balance of the Microverse« fahndet nach molekularen Angriffspunkten, um Parasiten wirksam bekämpfen zu können. Dabei geht es auch immer wieder darum, die Zusammenhänge zu verstehen, auf denen das Leben selbst basiert.
Text: Marco Körner
Parasiten können völlig verschiedene Lebewesen sein – von mehrzelligen Organismen, die außerhalb auf und an dem Wirtskörper leben, bis hin zu mikroskopisch kleinen Einzellern, die den Blutstrom bewohnen. »Faszinierend ist, dass diese Lebewesen in so unterschiedlichen Umgebungen leben können«, erklärt Prof. Dr. Ute Hellmich, die im Exzellenzcluster »Balance of the Microverse« forscht.
»Ein Parasit, der seinen Lebenszyklus in einem Wirt beginnt, beispielsweise in einem Insekt wie der Tsetse-Fliege, kann ganz andere Umgebungsbedingungen erfahren, wenn er auf einen anderen Wirt übertragen wird – zum Beispiel ein Säugetier. Dazu zählen die Temperatur oder der pH-Wert«, führt die Inhaberin der Professur für Biostrukturelle Interaktionen weiter aus. »Die Enzyme von Organismen sind normalerweise nur für bestimmte Umgebungen optimiert und sehr anfällig, was Schwankungen angeht. Umso erstaunlicher ist es, was diese Parasiten leisten.«
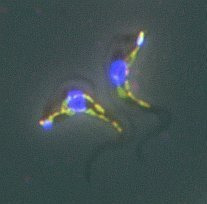
Fluoreszenzmikroskopische Aufnahme von Trypanosomen
Foto: Marta BogaczIn ihrer Forschung untersucht Hellmich unter anderem sogenannte Trypanosomen. Das sind einzellige Parasiten, die mit Wirtsorganismen, wie dem Menschen (oder auch seinen Nutztieren) interagieren, um sich in ihm zu etablieren und zu vermehren. »Trypanosomen verursachen Krankheiten wie die afrikanische Schlafkrankheit, Chagas-Krankheit oder Leishmaniose. Diese Krankheiten sind vor allem in tropischen und subtropischen Regionen verbreitet und führen oft zu schwerwiegenden gesundheitlichen Beeinträchtigungen«, führt Hellmich aus.
Dazu kämen soziale Stigmatisierungen, die das Leben der Erkrankten zusätzlich erschweren und belasten und eine ökonomische Komponente, da auch Nutztiere befallen werden können. »Wir wollen verstehen, wie sich solche Parasiten an unterschiedliche Lebensräume anpassen und mit Veränderungen umgehen, um molekulare Angriffspunkte in der Biochemie der Parasiten zu identifizieren, die in der Entwicklung neuer Medikamente genutzt werden können.« Ihr eigentlicher Fokus, erklärt die Wissenschaftlerin weiter, sei jedoch, die Zusammenhänge zu verstehen, auf denen das Leben selbst basiert, im Wirt und im Parasiten.
Auf die Details kommt es an
»So vielfältig das Leben auf unserem Planeten auch ist – auf molekularer Ebene basiert alles auf sehr ähnlichen biochemischen Mechanismen«, beschreibt Hellmich ihre Faszination für ihr Fach. »Genau deshalb lassen sich eben nicht einfach Medikamente entwickeln, die nur gegen den Krankheitserreger wirken, aber den Wirt nicht beeinträchtigen.« Hellmich und ihr Team suchen daher nach Biomolekülen, die nur im Erreger, aber nicht im Wirt vorkommen.
Das Enzym Tryparedoxin, das eine Schlüsselrolle im Redox-Stoffwechsel der Trypanosomen spielt, ist so ein Beispiel. »Tryparedoxin fungiert quasi als ›zentrales Zahnrad‹ im Stoffwechsel dieser Parasiten«, erläutert die Forscherin. »Es ist für die Reparatur von Zellstrukturen verantwortlich und unterstützt essenzielle Prozesse, die das Überleben und die Fortpflanzung der Parasiten ermöglichen.«
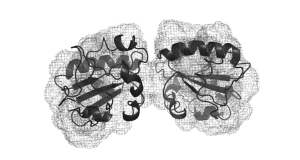
Struktur von zwei durch einen Inhibitor verklebten Tryparedoxinproteinen
Foto: Ute HellmichKrankheit bedeutet oft Stigmatisierung
Um dieses Enzym an der Arbeit zu hindern und den Krankheitserreger so zu eliminieren, entwickeln Ute Hellmich und ihre Gruppe »molekulare Klebstoffe« – Verbindungen, die an spezifischen Stellen des Enzyms ansetzen und bewirken, dass zwei Tryparedoxin-Moleküle miteinander verkleben und dadurch inaktiv werden. »Dieser Ansatz kann natürlich auch in anderen Bereichen der Zellbiologie genutzt werden «, sagt Ute Hellmich.
Gerade bei diesem Forschungsthema ist es den Forschenden wichtig, die Arbeit gut und verständlich zu vermitteln – sowohl, was die grundlegende Forschung angeht, als auch den gesellschaftlichen Kontext. »Von Krankheiten Betroffene erfahren oft zusätzliche Stigmatisierung, umso mehr, wenn sich Ausbreitungsgebiet und sozio-ökonomische Faktoren überlagern.«
Dies reiche von der Frage, für welche Krankheiten überhaupt Medikamente entwickelt werden und für wen solche Medikamente zugänglich sind, bis zum kompletten Ausblenden bestimmter Krankheiten, die Millionen Menschen betreffen – aber nicht im globalen Norden. »Wir bemühen uns, diese Zusammenhänge, neben der biochemischen Forschung, nicht aus den Augen zu verlieren und auch unseren Studierenden und der Öffentlichkeit zu vermitteln«, so Hellmich.
Das Ziel ihrer Arbeit bleibt jedoch vor allem, die Grundlagen des Lebens auf molekularer Ebene zu verstehen. »Die Erforschung der biochemischen Prozesse und molekularen Dynamik von Enzymen wie Tryparedoxin eröffnet nicht nur potenzielle Therapieansätze für Krankheiten, sondern trägt eben auch zur Beantwortung fundamentaler Fragen über die Funktionsweise des Lebens bei«, sagt die Wissenschaftlerin. Ihre Erkenntnisse sollen so nicht nur zum unmittelbaren Verständnis von Parasiten beitragen, sondern auch zum Wissen über die evolutionäre Vielfalt und Anpassungsfähigkeit des Lebens an sich.
Zellkulturflaschen an einem Laborarbeitsplatz
Foto: Anna Schroll07743 Jena Google Maps – LageplanExterner Link