Die Immunschwäche AIDS wird von HI-Viren verursacht, die Immunzellen - die sogenannten T-Helferzellen — außer Gefecht setzen. Statt andere Zellen des Immunsystems bei der Abwehr von Krankheitserregern zu steuern, produzieren infizierte T-Helferzellen neue HI-Viren in großer Menge. Einem internationalen Forschungsteam mit Jenaer Beteiligung ist es jetzt mithilfe höchstauflösender Bildgebung gelungen, in Echtzeit zu beobachten, wie sich HI-Viren zwischen lebenden T-Helferzellen verbreiten.
Mit der superauflösenden STED-Fluoreszenzmikroskopie (siehe Kasten unten) liefert das Forschungsteam einen direkten Beweis dafür, dass der AIDS-Erreger zum Vervielfältigen ein bestimmtes Lipidmilieu schafft. »Das liefert uns Anhaltspunkte zu erforschen, wie sich diese Vermehrung potenziell verhindern lässt«, sagt Prof. Dr. Christian Eggeling, der an der Friedrich-Schiller-Universität Jena, dem Leibniz-Institut für Photonische Technologien und der Universität Oxford forscht und lehrt.
Gemeinsam mit einem Team um Prof. Dr. Delphine Muriaux und Prof. Dr. Cyril Favard von der Université Montpellier und seinem Kollegen Dr. Jakub Chojnacki hat Christian Eggeling die Plasmamembran infizierter T-Helfer-Zellen untersucht. In den Fokus nahmen die Forschenden dabei die »Schleuse«, durch die das HI-Virus (Human Immunodeficiency Virus) aus der Zelle heraustritt, nachdem es sich darin vermehrt hat. Als Marker diente ihnen dabei das Protein »Gag«, das die Vorgänge beim Zusammenbau der neu produzierten Viruspartikel koordiniert. »Dort, wo sich dieses Protein sammelt, laufen die entscheidenden Prozesse ab, die dazu führen, dass die Viren sich freisetzen und weitere Zellen infizieren«, erläutert Christian Eggeling. Um diese Prozesse zu entschlüsseln, haben sich die Forschenden die Diffusion des »Gag«-Proteins an den Ort der Knospung - des »budding« - des Viruspartikels angesehen. Während des »budding« treten die Viruspartikel durch die Plasmamembran aus der Zelle und erhalten dabei ihre Lipidhülle. Wie Eggeling und seine Kollegen nun herausgefunden haben, wechselwirken nur ganz bestimmte Lipide aus der Zellmembran mit dem HI-Virus. Zwar waren diese Lipide prinzipiell schon vorher bekannt, aber das Forschungsteam konnte diese Wechselwirkung nun erstmals direkt in lebenden Zellen beobachten.
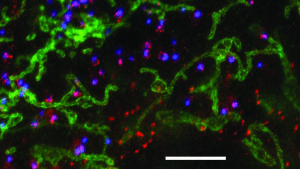
STED-Mikroskopie-Aufnahme von Fibroblastenzellen. Der weiße Balken ist fünf Mikrometer lang.
Foto: Christian Eggeling»Damit haben wir einen potenziellen Angriffspunkt, an dem antivirale Medikamente ansetzen könnten«, so Christian Eggeling. »Zu wissen, welche Moleküle das HI-Virus braucht, um aus der Zelle herauszutreten und sich zu vervielfältigen, ist eine entscheidende Voraussetzung, um zu erforschen, wie sich dies verhindern lässt. Mit unserer Technik können wir das jetzt direkt und live verfolgen.« Mit seinem Team will Eggeling nun Antikörper entwickeln, die genau diese Moleküle angreifen - und so die Verbreitung des Virus unterdrücken.
Bewegung von Molekülen
in Echtzeit verfolgen
»Wir wollen diese Antikörper nicht nur in medizinischer Hinsicht untersuchen, sondern herausfinden, wie man ihre biophysikalische Wechselwirkung nutzen kann, um ihre Wirksamkeit zu verstärken«, kündigt Eggeling an. Um auf molekularer Ebene zu verstehen, wie Krankheiten entstehen, kombiniert Eggeling superauflösende Fluoreszenzmikroskopie-Techniken mit Methoden, die die Bewegung markierter Moleküle in Echtzeit verfolgen. So lassen sich einzelne Moleküle in lebenden Zellen räumlich und zeitlich untersuchen. »Das ermöglicht es uns, zelluläre Mechanismen auf molekularer Ebene zu enthüllen, die für bisherige Untersuchungsmethoden viel zu schnell sind und auf viel zu kleinen räumlichen Skalen ablaufen.«
Text: Lavinia Meier-Ewert
| STED steht für »Stimulated Emission Depletion« und ist ein fluoreszenzmikroskopisches Verfahren, mit dem die von Ernst Abbe beschriebene optische Auflösungsgrenze unterschritten werden kann. Bei dem Verfahren werden Fluoreszenz-Farbstoffe durch Licht angeregt, die anschließend spontan Licht in einem energieärmeren Wellenlängenbereich abstrahlen. Diese spontane Abstrahlung lässt sich unterdrücken, wenn intensives Licht dieser energieärmeren Wellenlänge zusätzlich eingestrahlt wird. Das Abregungslicht wird ringförmig um den Fokus der zu untersuchenden Probe gelegt, wodurch sich die Emission von Fluoreszenzlicht auf den zentralen Bereich der Probe beschränkt. Dieser effektive Fokuspunkt ist durch diesen optischen Trick erheblich verkleinert und seine Ausdehnung liegt unterhalb der Abbeschen Beugungsgrenze. |
Original-Publikation: HIV-1 Gag specifically restricts PI(4,5)P2 and cholesterol mobility in living cells creating a nanodomain platform for virus assembly. Science Advances (2019), DOI: 10.1126/sciadv.aaw8651Externer Link